Leeftijd is meer dan een getal: De determinanten van verouderen
Vaccineren tegen veroudering
Door Eva Dekker
Afgelopen december hadden Japanse wetenschappers aan de Juntendo Universiteit een wereldprimeur te pakken: Het team kwam naar buiten met een onderzoek waarin ze muizen succesvol vaccineerden tegen ‘zombiecellen’ oftewel onze verouderingscellen. Dit nieuws ging al snel de wereld over: David Sinclair, een vooraanstaande bioloog in de verouderingswetenschap, tweette erover en zei: “Okay, this is a big deal. (…) there’s little doubt this will be possible in us one day.”
Dit is het eerste onderzoek waarin het doden van deze cellen middels vaccinatie wordt gedaan. Behandelingen tegen verouderingscellen, ook wel senolytics genoemd, worden al wel langere tijd ontwikkeld. Peter de Keizer is onderzoeker aan het UMC Utrecht en bestudeert zombiecellen al jaren. In 2017 ontwikkelde hij zelf een senolytic die hij binnenkort naar de mens wil brengen. De Keizer is terughoudend over het Japanse onderzoek, maar verwacht wel dat senolytics in de toekomst een groot deel van de oplossing vormen voor verouderingsproblemen.
Veroudering veroorzaakt ziekte
Om te begrijpen hoe onze zombiecellen zorgen voor veroudering, is het belangrijk om duidelijk te hebben wat we verstaan onder veroudering en het remmen ervan. Veroudering is meer dan uiterlijke kenmerken; het gebeurt in onze cellen en in onze organen, waardoor onze lichaamsfuncties langzaam achteruitgaan. Kanker, Alzheimer, hart- en vaatziekten, allemaal hebben ze één ding gemeen: Je krijgt ze meestal niet voor je dertigtse levensjaar. Veroudering is de oorzaak van ontzettend veel ziektes. Hoe kan dit?
Zombiecellen hopen op in je lichaam en zijn schadelijk
Tijdens je leven delen en vernieuwen de meeste cellen in je lichaam continu. Hierbij kunnen ze schade oplopen. Wanneer de schade te ernstig is om te repareren, stimuleert je lichaam de beschadigde cel om gecontroleerd ‘zelfmoord’ te plegen. Maar naarmate je ouder wordt, gaat dit steeds slechter. De cellen delen dan niet, maar plegen ook geen zelfmoord. Ze blijven beschadigd in je lichaam zitten. Wetenschappers noemden de cellen daarom senescente cellen, naar het Latijnse woord ‘senex’, wat oud betekent.
In 2008 ontdekte het Amerikaanse lab waar de Keizer destijds werkte een belangrijke kwaadaardige functie van senescente cellen: ze scheiden schadelijke stofjes uit die de cellen om hen heen ook beschadigt. Doordat deze cellen zich ophopen met leeftijd, krijg je steeds meer schade in je lichaam en grotere kans op ziekte. Door die eigenschap, in combinatie met het weigeren om te sterven, kregen senescente cellen in het nieuws de bijnaam ‘zombiecellen’.
Doden van zombiecellen
Senolytics is de verzamelnaam voor stofjes die gericht zijn op het specifiek doden van zombiecellen. Elk hebben ze hun eigen doelwit en werking. Ze stimuleren de cellen die weigeren dood te gaan om toch zelfmoord te plegen (zie afbeelding hieronder). De senolytic die De Keizer maakte, testte hij op snel verouderende muizen. Met gunstige resultaten: de muizen werden fitter en hun haar groeide weer terug. Dat belooft veel voor de mens: “Kijk naar een auto,” aldus de Keizer. “Als het linkerwiel ermee ophoudt, vervang je dat. Een mens overlijdt nu aan één onderdeel. Het vervangen van onze verroeste onderdelen kan nu nog niet, maar daar gaan we denk ik wel naartoe.” Die vergelijking is natuurlijk wat scheef; senolytics zijn niet de manier om menselijke onderdelen te vervangen. Maar het verwijderen van onze ‘roest’ maakt al veel verschil voor onze gezondheid.
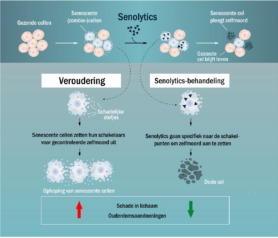
Een schematische weergave van de werking van senolytics. Senolytics moeten specifiek zijn voor senescente cellen (boven) en gaan verslechterde gezondheid als gevolg van ouderdom tegen (onder). Bewerkt van Kirkland, 2020.
Niet langer leven, maar gezonder leven
Een ontroestingsbehandeling dus. Dat wordt in de toekomst hard nodig, zegt de Keizer: “In 2040 zullen we in Nederland evenveel 65-minners als 65-plussers hebben. Als we niks doen, krijgen we teveel zorgbehoevende ouderen ten opzichte van te weinig werkende jongeren. De zorgkosten zullen te hoog worden en de samenleving zal veel problemen krijgen.” En wat kunnen senolytics hieraan doen? “In Europa hebben mensen gemiddeld 20 zieke jaren, dat wil zeggen: jaren waarin je 2 of meer ouderdomsaandoeningen hebt. Je hebt in de wereld een aantal ‘blue zones’ waar mensen – zonder gebruik van senolytics – met maar 3 zieke jaren leven. Daar moeten wij ook naartoe.” Dat moeten senolytics dus doen: Toevoegen van gezonde jaren, niet levensjaren.
Is het Japanse vaccin-onderzoek dan nu dé doorbraak in gezond ouder worden? Dat is nog niet te zeggen. Het middel is nu niet specifiek genoeg voor alleen senescente cellen. En daarmee kent het vaccin een groot risico, aldus de Keizer: “Vaccineren betekent hier dat je je immuunsysteem traint om je eigen cellen aan te vallen.” Dat is gevaarlijk wanneer het stofje waartegen het vaccin je immuunsysteem traint niet alleen op senescente cellen zit, maar ook gezonde cellen. Dat is in dit Japanse onderzoek ook het geval. “Dan zou de kans op auto-immuunziektes ook verhogen.” Daarom is een vaccin dat op deze manier werkt waarschijnlijk geen geschikte manier om onze zombiecellen aan te pakken. Gaan de onderzoekers toch door met dit vaccin, dan moeten ze op één ding heel goed testen: veiligheid.
Voorlopig zal het nog even duren voordat een anti-verouderingsmiddel de markt bestormt. Voor het ontwikkelen van een veilig middel zijn vaak jaren aan klinische studies nodig. De Keizer hoopt binnen 25 jaar een anti-senescence middel op de markt te zien. Maar voor het zover is, weet hij ook andere manieren te noemen om de ophoping van zombiecellen zoveel mogelijk te beperken: “Zoals Cicero 2000 jaar geleden al zei: een goede dag krijg je door te zorgen voor je intellect, goede beweging en niet teveel te eten.” Zo zie je maar: gezond oud worden begint bij jezelf.
Bronnen:
- Interview Dr. Peter de Keizer
- https://longreads.cbs.nl/european-scale-2019/life-expectancy/
- https://data.worldbank.org/indicator/SP.DYN.LE00.FE.IN?locations=NL
- Suda, M., Shimizu, I., Katsuumi, G., Yoshida, Y., Hayashi, Y., Ikegami, R., Matsumoto, N., Yoshida, Y., Mikawa, R., Katayama, A., Wada, J., Seki, M., Suzuki, Y., Iwama, A., Nakagami, H., Nagasawa, A., Morishita, R., Sugimoto, M., Okuda, S., … Minamino, T. (2021). Senolytic vaccination improves normal and pathological age-related phenotypes and increases lifespan in progeroid mice. Nature Aging, 1(12), 1117–1126. https://doi.org/10.1038/s43587-021-00151-2
- https://pubmed.ncbi.nlm.nih.gov/32686219/

