Kunstorganen in de maak
Piepkleine chip kan straks de behandeling voor nierfalen verbeteren
In Nederland hebben zo’n 1,5 miljoen mensen een vorm van nierschade. De ernstigste 6500 gevallen worden meestal behandeld met dialyse, maar dat werkt lang niet goed genoeg: jaarlijks overlijdt één op de zes dialysepatiënten. Daar komt binnenkort misschien verandering in. Een Duits-Nederlands-Vlaams-Amerikaans onderzoeksteam heeft dit jaar namelijk een speciale chip gepresenteerd die de behandeling van een slecht werkende nier (nierfalen) kan verbeteren. Hoe werkt deze chip precies? En hoe ziet de toekomst van de chip eruit?
Door Merel Smid
“Eigenlijk persen we een tafel vol apparatuur in een piepkleine chip, die helpt bij het zuiveren van het bloed tijdens dialyse,” vertelt dr. Fokko Wieringa enthousiast. Hij is onderzoeker bij Stichting IMEC Nederland en maakt onderdeel uit van de onderzoeksgroep achter de nier-chip.
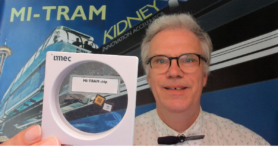
Dr. Wieringa met de chip (foto IMEC Nederland)
De chip moet ervoor zorgen dat een dialysebehandeling beter wordt in het nabootsen van een echte nier. “Gezonde nieren verwijderen afvalstoffen en een teveel aan water uit ons bloed en scheiden dat uit in de urine,” aldus Wieringa. Deze afvalstoffen zijn bijvoorbeeld restproducten van de spijsvertering, waar het lichaam niks mee doet. Je kunt je een nier dus ook wel voorstellen als een soort zeef: deze zuivert het bloed, terwijl de nuttige stoffen worden behouden. De nieren zijn hier dag en nacht mee bezig. Maar wat als ze niet goed meer kunnen functioneren? “In dat geval is de verwijdering van afvalstoffen sterk verminderd. Hierdoor hoopt het afval op in het bloed. Dit beschadigt onze organen en maakt ons ziek.” Hierbij kun je denken aan vermoeidheid, verminderde concentratie of bot- en longproblemen. Een goede nierfunctie is dus van groot belang.
Een behandeling met gebreken
Helaas komt nierfalen behoorlijk vaak voor. Elk jaar komen er in Nederland ongeveer 2000 nierpatiënten bij. Wanneer nierfalen onbehandeld blijft, is dit dodelijk. “Als de nierfunctie onder de 15% komt, heb je óf niertransplantatie óf dialyse nodig om in leven te blijven,” geeft Wieringa aan. “Transplantatie is verreweg de beste optie, maar er is een tekort aan nieren van donoren. Daarnaast is niet elke patiënt geschikt voor transplantatie. Daarom vormt dialyse de voornaamste steunpilaar in de behandeling tegen nierfalen.”
Tijdens een dialysebehandeling wordt het bloed van de nierpatiënt via slangen in een uitwendige machine (het dialyse-apparaat) geleid. Dit apparaat lijkt, net zoals een echte nier, op een zeef: het filtert schadelijke afvalstoffen uit het bloed en leidt het gezuiverde bloed vervolgens terug naar het lichaam. Tijdens zo’n sessie, die ongeveer vier uur duurt, kan de patiënt bijvoorbeeld lezen, muziek luisteren of slapen. De meeste patiënten ondergaan drie dialyse-sessies per week. Hiervoor moeten ze naar het ziekenhuis of een gespecialiseerde kliniek.
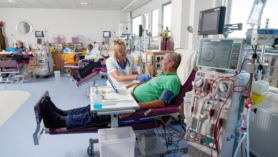
De meest gebruikte behandeling voor nierfalen: dialyse (foto Nierstichting)
Hoewel dialyse nierpatiënten in leven houdt, kleven er behoorlijk wat nadelen aan: het is bijvoorbeeld vermoeiend voor de patiënt en kan maar zeer gedeeltelijk de functie van een echte nier overnemen. En dat heeft zo zijn gevolgen. “Dialyse-patiënten hebben een beperkte levensverwachting. Binnen 5,5 jaar overlijdt 70% van hen. Hun kans op hartproblemen is veel hoger in vergelijking met leeftijdsgenoten die geen dialyse ondergaan. Elke verbetering binnen de behandeling voor nierfalen is daarom extreem belangrijk.”
Afvalstoffen lostrillen
Het feit dat dialyseapparaten slechter werken dan gezonde nieren, wordt vooral veroorzaakt door een bepaald type afvalstoffen in het bloed. “In hun eentje passen zij door de zeef-achtige structuur van een dialyseapparaat, maar 95% van de tijd plakken ze vast aan bloedeiwitten,” legt Wieringa uit. Bloedeiwitten zijn nuttige stoffen in het bloed met allerlei functies: ze zijn bijvoorbeeld betrokken bij de bloedstolling. Op het moment dat de afvalstoffen aan bloedeiwitten vastplakken, kunnen ze niet door de ‘zeef’ van het dialyseapparaat heen en worden ze dus niet uit het bloed verwijderd. Daardoor hopen deze afvalstoffen op en blijven ze hun schadelijke effecten uitoefenen op het lichaam.
Dit is precies waar dr. Wieringa en zijn collega’s verandering in wilden brengen. Ze vroegen zich dan ook af: hoe kunnen we de kleine afvalstoffen uit het bloed zuiveren, terwijl we de nuttige bloedeiwitten behouden? Het antwoord hierop kwam uit een ziekenhuis in het Duitse Aken. Daar ontdekte men dat je radiogolven – een vorm van elektriciteit én magnetisme – kunt gebruiken om de kleine afvalstoffen los te trillen van de bloedeiwitten waar ze aan vast plakken. Op die manier kunnen de afvalstoffen wél uit het bloed worden gefilterd tijdens dialyse. “De elektronica die hiervoor nodig is, heeft IMEC op een chip weten te persen. Deze wordt gemaakt in de IMEC-fabriek in Leuven. Het resultaat is zo klein dat het op mijn vingertopje past,” licht Wieringa toe. “Verpleegkundigen kunnen de chip straks simpelweg op de slangen van een bestaand dialyseapparaat vastklemmen.”
Toekomst
Voorlopig zal de chip nog niet in het ziekenhuis gebruikt worden. Eerst heeft de onderzoeksgroep tijd nodig om het systeem te testen. “Dat doen we eerst op geiten met nierfalen, daarna op mensen.” Hiermee bekijkt de onderzoeksgroep de werkzaamheid en veiligheid van de chip. “Vervolgens gaan we de chip aanbieden aan partijen die het willen uitproberen op bestaande dialyse-apparaten,” zoals gespecialiseerde klinieken, “maar ook aan wetenschappers die bezig zijn met het ontwikkelen van kunstnieren (die je in het lichaam kunt plaatsen, red.). Zij kunnen goed profiteren van de kleine omvang van onze chip.”
Kortom: de resultaten van Wieringa en zijn collega’s zijn tot nu toe veelbelovend. De eerste chips zijn inmiddels gemaakt, maar nu is het nog afwachten of de volgende testfases goed verlopen. Is dat het geval, dan gloort er voor zo’n dialysepatiënten wereldwijd wat meer licht aan de horizon.
De opmerkingen van dr. Wieringa zijn verkregen uit zijn pitch voor de wetenschappelijke KidneyX-prijs, te vinden op deze website.
Bronnen
https://www.nhs.uk/conditions/dialysis/what-happens/
https://www.radboudumc.nl/nieuws/2016/een-stap-dichterbij-de-biologische-kunstnier
https://www.utwente.nl/uwgezondheidonzetechnologie/biologische-kunstorganen-biorobotica
Van Gelder, M. K., Mihaila, S. M., Jansen, J., Wester, M., Verhaar, M. C., Joles, J. A., Stamatialis, D., Masereeuw, R., & Gerritsen, K. G. F. (2018). From portable dialysis to a bioengineered kidney. Expert Review of Medical Devices, 15(5), 323–336. https://doi.org/10.1080/17434440.2018.1462697
Vanholder, R., Annemans, L., Bello, A. K., Bikbov, B., Gallego, D., Gansevoort, R. T., Lameire, N., Luyckx, V. A., Noruisiene, E., Oostrom, T., Wanner, C., & Wieringa, F. (2021). Fighting the unbearable lightness of neglecting kidney health: the decade of the kidney. Clinical Kidney Journal, 14(7), 1719–1730. https://doi.org/10.1093/ckj/sfab070

